近日,生命学院沈锡辉教授团队在《Nature Communications》发表了题为“Autoinducer-2 and bile salts induce c-di-GMP synthesis to repress the T3SS via a T3SS chaperone”的研究论文,揭示了细菌群体感应信号AI-2及胆汁酸盐作用于跨膜二鸟苷酸环化酶刺激细菌胞内第二信使c-di-GMP合成,进而通过作用于c-di-GMP分子靶标T3SS伴侣蛋白抑制T3SS活性的分子机制。生命学院博士后李书宇,硕士生孙恒玺为本论文共同第一作者,张磊教授、沈锡辉教授,以及福建师范大学欧阳松应教授为本论文的共同通讯作者。
环二鸟苷单磷酸(c-di-GMP)是细菌中广泛存在的一类核苷类第二信使,能够调控细菌的生物被膜形成、胞外多糖产生、运动性、黏附以及毒力等众多生理和病理过程。III型分泌系统(T3SSs)是大多数革兰氏阴性病原细菌感染宿主的重要武器。病原菌通过T3SSs将一系列效应蛋白注入宿主细胞内,逃避宿主细胞的免疫防御并建立感染。T3SSs基因的表达受各种环境和宿主因素的影响,也受到c-di-GMP信号途径的调控,但具体分子机制尚不清楚。
群体感应(quorum sensing,QS)是细菌种内和种间细胞间交流的普遍机制。沈锡辉教授团队前期研究发现QS信号分子autoinducer-2 (AI-2)通过作用于一类具dCACHE结构域的跨膜二鸟苷酸环化酶提高其c-di-GMP合成酶活性(Zhang et al., Nature Communications, 2020),并基于这一类AI-2新受体构建了瘤胃微生物种间交流网络(Liu et al., Microbiome, 2022)。胆汁酸盐是肝细胞合成的初级胆汁酸经肠道细菌共同参与代谢后在肠道内形成的一系列胆烷酸钠盐或钾盐物质,其不仅影响肠道的消化吸收等功能,也能够调控肠道细菌的生理和代谢活动。
本研究中,研究人员发现AI-2通过作用于具GAPES1结构域的跨膜二鸟苷酸环化酶YeaJ促进沙门氏菌胞内c-di-GMP水平的提升,从而抑制其T3SS-1基因的表达。随后的研究表明具GAPES1结构域的跨膜二鸟苷酸环化酶是一类AI-2新受体,在肠杆菌目革兰氏阴性细菌中广泛存在。此外,研究人员发现肠道胆汁酸盐组分牛磺胆酸盐和牛磺脱氧胆酸盐作用于跨膜二鸟苷酸环化酶YedQ,刺激沙门氏菌胞内c-di-GMP合成,也能抑制其T3SS-1基因表达。进一步研究发现c-di-GMP通过作用于沙门氏菌T3SS-1的CesD/SycD/LcrH家族伴侣蛋白SicA抑制T3SS-1基因表达,且发现许多其它革兰氏阴性病原菌(包括肠出血性大肠埃希杆菌、铜绿假单胞菌、弗氏志贺菌、小肠结肠炎耶尔森氏菌、泰国伯克霍尔德菌、副溶血性弧菌等)中该家族T3SS伴侣蛋白也是c-di-GMP的作用靶标。本研究揭示了c-di-GMP通过保守的分子机制来调控病原细菌T3SSs的活性,丰富了对c-di-GMP信号代谢、受体感应及调控机制的认知,同时为抗细菌感染药物研发提供了新靶点。
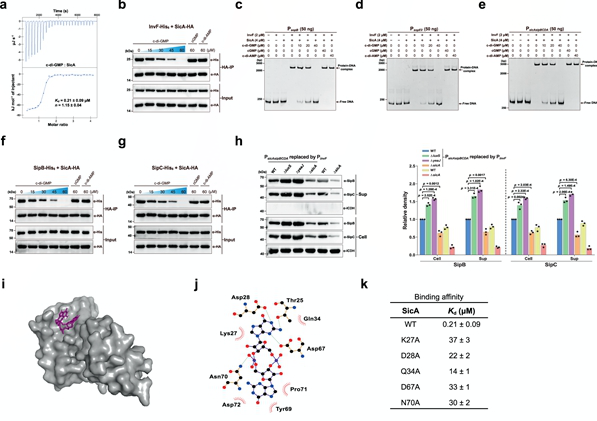 图1. c-di-GMP作用于沙门氏菌T3SS伴侣蛋白SicA抑制T3SS基因表达
图1. c-di-GMP作用于沙门氏菌T3SS伴侣蛋白SicA抑制T3SS基因表达
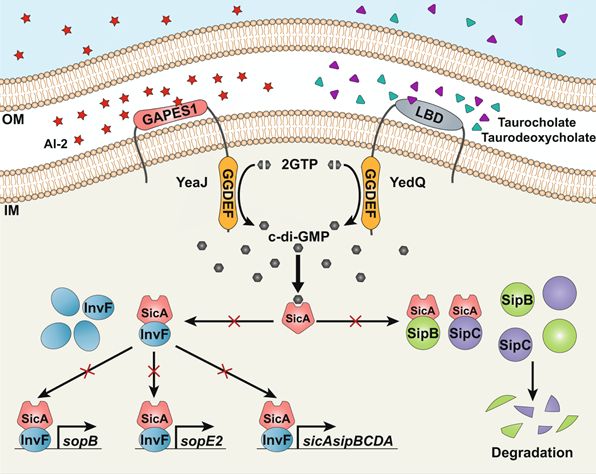 图2. AI-2与胆汁酸盐通过c-di-GMP信号途径调控T3SS活性的分子机制
图2. AI-2与胆汁酸盐通过c-di-GMP信号途径调控T3SS活性的分子机制
该研究得到了国家自然科学基金和国家重点研发计划的资助。
文章链接:https://www.nature.com/articles/s41467-022-34607-9
编辑:张晴
终审:徐海